Таким вопросом задается любая женщина, даже если это не в первый раз, поскольку каждая беременность уникальна по наличию тех или иных признаков.
Вместе со Светланой Андреевной Чупиной, врачом акушером-гинекологом 4 Роддома ГКБ № 31 им. Савельевой
экспресс анализ крови на хгч
Обновлено:
Начну с того, что мне 31 год, беременность первая и очень желанная.
Примерно год назад поговорили с мужем и решили, что пора, пора нам стать родителями. Оп, задержка, но тесты отрицательные. В замешательстве бегу к врачу, а там «ановуляторный цикл». Я так расстроилась, а врач говорит «Я тебе сейчас назначу препарат, мигом залетишь!»
Шел второй месяц 2024 г.
Февраль 2024
10 февраля.Начался новый цикл, звонок в клинику для записи к Ре. Ждут 12.02 , записали к Ре и сразу в договорной отдел для подписи договора о вступление в крио-протокол. Хороший знак.
12.02 . Утром сбегала сдать гормоны. Вечером в клинику.
Ожидая приема, я практически не нервничал
После родов прочитав свою выписку я опешила. Шейку матки слаживали. В общей сложности 18 швов (1 наружный, 1 внутри матки, 16 на шейка матки).
Проходит год и мы задумываемся о втором. И тут опять качели. 4 выкидыша. За 2 года. В перерывах между не...
Мне 28лет. Собственно говоря это моя первая беременность..Итак..
Мы с мужем женаты уже 3года, живём вместе 5 лет. Стоит сказать, что цикл у меня нестабильный. Почти сразу после свадьбы мы решили стать родителями, пытались более полгода, я вела календарь,...
Рассмотрены возможные причины привычной потеря беременности, включая генетические, эндокринные и иммунологические, подходы к диагностике и ведению пациенток, методы и профилактики преждевременных родов.
Подготовка к протоколу
Обычно начинается за 2-3 месяца до протокола.
1. Пьем витамины для беременных с фолиевой кислотой: Элевит, Фемибион (для тех, у кого есть неусвоение фолиевой кислоты по анализам на риск невынашиваемости и повышенный гомоцистеин), Ангиовит.
2. Улучшаем состав крови и кровоснабжение органов: Омега-3, Курантил, Актовегин, Вобензим.
3. Улучшаем работу яичников, снижаем ФСГ, улучшаем качество эмбрионов:
- Уколы гомеопатии фирмы «Хелл» по схеме: Овариум композитум, Убихинон композитум, Коэнзим композитум - каждый день начиная с 4ДЦ по 1 уколу, потом день перерыв, и все сначала. Колоть 2 цикла.
- Цитамины: за 1-2 мес до протокола и в протоколе до пункции: Овариамин (для яичников) - 6т. в день; Эпифамин (для иммунки) - 4т. в день; Тиммусамин (для сосудов, крови) - 4т. в день. Также помогают снизить ФСГ и нормализовать цикл - Циклодинон, Цикло-Прогинова.
4. Для профилактики воспалений мочеполовой сферы пьем отвары/настои трав боровой матки и красной щетки.
5. Для профилактики цистита и болезней почек: цитамин Ренисамин, гомеопатия фирмы «Хелл» Популюс композитум, Канефрон (можно беременным и в протоколе).
6. Для рассасывания спаек, улучшения эндометрия, для подлечивания аденомиоза и хронического эндометрита (ХЭ): свечи или уколы Лангидазы, прием Индинола.
7. Лечим эндометриоз и аденомиоз:
- Радоновые ванны (нельзя при СИЯ (синдром истощения яичников), при проблемах со щитовидкой, например, при гипотиреозе). Есть в 122 МСЧ, в санаториях Белоруссии.
- Пьем ОК (Марвелон, Логест и пр.), уходим в искусственный климакс (ИК).
8. Лечим ХЭ: 3 укола современного иммуномодулятора Натрия нуклеоспермат (болючие). Можно ректально, но лечиться 1-1,5 месяца. Эффект очень хороший.
9. Ставим пиявки: при миомах, кистах, проблемах эндометрия, для улучшения параметров крови. Ставятся на крестец, живот и во влагалище.
Есть пример излечения миомы после 2х курсов пиявок.
10. Иглоукалывание лечит всё, и особенно ИЯ (есть примеры ЕБ после курса) -
11. Для улучшения кровотока в матке за месяц до протокола полезно упражнение по сжиманию мышц малого таза и ануса 5-10 мин в день (улучшает яичники, рассасывает кисты и миомы).
12. Для очистки печени между протоколами: 5-7 капельниц Гептрала. Биохимия после него идеальна, он оказывает и противоспаечное действие. Особо хорошо после операций. В таблетках особо сильного воздействия не оказывает.
Еще для печени хорошо: Зифлан, Карсил, Расторопша, Овесол.
Для мужей, особенно у кого плохая сперма:
1. Омега-3, витамины с фолиевой кислотой, L-карнитин, Верде (масло пшеницы).
2. Нельзя париться в бане и лежать в горячей ванне за 1 мес до протокола.
3. С начала протокола и до пункции пить апельсиновый сок или принимать витамин С (улучшает подвижность), есть больше креветок и рыбы (йод).
Анализы и обследования
Обычные анализы можно быстро сдать в лабораториях НИИАП (обращаться в окошко Платные услуги - там дешевле), Евродон, НАУКА, Новые Медицинские Технологии.
Анализы по гемостазу (агрегация, гомоцистеин и пр.), иммунные и генные анализы: НИИАП, ОКДЦ.
Проверка системы гемостаза: проверяем, если нет имплантации или были ЗБ. Можно проверить и перед первым протоколом.
Для первичного посещения гематолога при подозрении на проблемы крови нужно сделать: расширенную коагулограмму, клинический анализ крови, д-димер, агрегацию тромбоцитов.
Система гемостаза - биологическая система, обеспечивающая, с одной стороны, сохранение жидкого состояния циркулирующей крови, а с другой - предупреждение и купирование кровотечений.
1. Сдаем на полиморфизмы (мутации) генов системы гемостаза. Основных генов 7 + 2 по части гомоцистеина (гомоцистеин влияет на способность организма усваивать фолиевую кислоту, которая крайне важна для развития нервной системы ребенка в утробе матери).
2. Сдаем кровь на
- д-димер
- агрегацию тромбоцитов
- расширенную коагулограмму
- гомоцистеин
3. С результатами проконсультироваться у гематолога. Можно обратиться:
Вагнер Лариса Владимировна ОКДЦ.
В случае, если будут обнаружены отклонения в с-ме гемостаза, нужно будет корректировать кровь во время протокола:
Сдавать кровь на 5-7 день стимуляции и после переноса, как можно будет встать (на 3-5 ДПП). После консультации гематолога принимать лекарства, прописанные доктором. Чаще всего прописывают уколы Фраксипарина, прием Аспирина.
Расширенная коагулограмма (гемостазиограмма):
Протромбиновое время
Протромбиновый индекс
АПТВ индекс (АЧТВ)
Тромбиновое время
Фибриноген
МНО
Волчаночный антикоагулянт
Антитромбин
Агрегация тромбоцитов и Д-димер - показывают есть ли микротромбы, что может повлиять на имплантацию и выкидыш на ранних сроках.
Гомоцистеин - если повышен, то может не быть развития или серьезные неврологические проблемы у ребятенка.
Анализы для проверки иммунного статуса:
Делаем HLA-типирование 2 класса (Аш-Эль-А-типирование) - система генов тканевой совместимости супругов
Очень подробно и понятно об этом можно почитать в статье Б.А. Каменецкого, размещенной на форуме русмедсерв.ком - прогуглите по запросу "HLA совпадения. ЛИТ - делать или нет? СКЛ - как правильно?". Так же рекомендуем ознакомиться с мнением на эту тему П.А. Базанова, интервью размещено на сайте "Ассоциации пациентов ВРТ", тоже можно найти через поисковик (давать ссылки на сторонние инет-ресурсы, посвященные ЭКО, ВРТ, медицине, фармацевтике и т.п. на Пробирке запрещено).
Нам нужны локусы HLA-DRB1, HLA-DQB1 HLA-DQA1. В каждом локусе по две аллели. Сравнивая аллели в каждом локусе у мужа и жены, врач приходит к выводу о количестве совпадений - их может быть от 0 до 6, соответственно. Если совпадений 2 и менее - забудьте об этом и живите дальше. Если 3 и более - может понадобиться иммунная коррекция (лимфоцитоиммунотерапия (ЛИТ) и/или применение иммуноглобулинов).
Фактически совпадения означают, что малыш может получиться слишком похожим на мамин организм, тогда может вовремя не включиться правильный механизм сохранения беременности, мамина иммунная система может решить, что это вовсе не малыш, а измененные мамины клетки (т.е. опухоль) - и вызвать отторжение плода.
В любом случае, после получения результатов анализа главное - найти грамотного иммунолога, который прокомментирует ответ и порекомендует, что делать.
Нужно отметить, что многие врачи и ученые считают эту область крайне малоизученной и не придают значения этому анализу. Генов, влияющих на тканевую совместимость, в человеческом организме более 200, а тут исследуются всего 3 и делаются такие глобальные выводы.
Анализы для проверки генных проблем невынашиваемости:
Диагностика первичного антифосфолипидного синдрома (АФС):
Наличие АФС является частой причиной неудачных ЭКО и невынашивания.
Антинуклеарный фактор на клеточной линии HЕp-2 с определением 6 типов свечения
антитела к бета-2-гликопротеину I класса IgG
Антитела к кардиолипину класса IgG
Антитела к кардиолипину класса IgM
Риск невынашивания беременности и патологии плода (исследуется 15-17 полиморфизмов) - сюда же входит и исследование с-мы гемостаза, описанное выше.
Вот эти 17 генов на невынашивание беременности и патологии плода:
1) свертывающая система крови (6 генов)
2) нарушение тонуса сосудов (2 гена)
3) репродуктивное здоровье (1 ген)
4) сис-ма детоксикации, биотрансформации (3 гена)
5) метаболизм гомоцистеина (2 гена)
6) HLA-система (3 пункта, 2й класс)
Ну и если есть отклонения по этим генам - то далее к гематологу/иммунологу.
Выглядят эти анализы примерно так:
Молекулярно-генетическое типирование факторов системы гемостаза:
1) мутация в гене фактора V (FV Leiden)
2) мутация 20210G -> A в гене протромбина
3) полиморфизм - 675 4G -> 5G в гене PAI-1
4) полиморфизм - 455 G -> A в гене бетта-субъединицы фактора I
5) полиморфизм 1565 T -> C (A1/A2, HPA-1) в гене GpIIIa
6) полиморфизм 434 T -> C (2A/2B, HPA-2) в гене GpIba
7) полиморфизм 807 C -> T в гене GpIa
8) 677 C -> T в гене метилентетрагидрофолат редуктазы (MTHFR)
9) 66 A -> G в гене метионин синтазы редуктазы (MTRR)
Два последних гена на усвоение фолиевой кислоты, если они с мутациями велика вероятность гипергомоцистеинемии.
Что делаем в протоколе
1. Едим белковую пищу, кроме кур и грибов. Такая диета предупреждает синдром гиперстимуляции яичников (СГЯ).
К допустимым при ЭКО продуктам относят кролика, индейку и рыбу в любом виде. Подойдут также сыр, творог, йогурт и другие молочные продукты. Как источник калия и кальция можно выбрать сухофрукты - в особенности курагу, изюм и чернослив. Также рекомендуется зелень - петрушка и укроп.
Во время проведения ЭКО требуется полностью исключить из рациона продукты, вызывающие метеоризм и вздутие живота. Не рекомендуются продукты, богатые углеводами - картофель и сладкие мучные изделия.
Пациентам ЭКО следует к тому же ограничить потребление соли. С целью улучшения стула возможно потребление клетчатки.
2. При стимуляции овуляции, после пункции и переноса эмбрионов пьем до 2-3 литров в день простой негазированной воды. Также не рекомендуются напитки, содержащие кофеин - кофе, крепкий чай, кока-кола и другие.
3. Витамины в протоколе обычно не пьем (кроме прописанных для крови).
4. Для лучшего наращивания эндометрия пьем тыквенный сок (детское питание или свежевыжатый), едим тыкву. Пьем чай с листьями малины (2-3 листа на чашку), едим морепродукты.
5. Перед подсадкой за 1 день пьем Пироксикам 10 мг (расслабляет матку) - 1 таблетка 3 р./д. за сутки до переноса и в день подсадки 1 таб. за 2 часа до переноса.
6. При тянущих болях в матке пьем Но-шпу (до 6 таблеток в день), ставим свечи Папаверин и пьем МагнеB6.
Если начало мазать в протоколе или на первых неделях беременности:
Очень большой процент ЭКО беременностей сопровождается кровотечением разной степени тяжести, особенно в первые 12 недель, без отрицательных последствий для малыша. При появлении выделений нужно позвонить врачу.
Не паниковать, выпить Валерианы или Персена, лежать.
Если до врача не дозвониться:
Увеличить поддержку: добавить Прогинову 1 т. (или Дивигель 1 пакетик) и укол Прогестерона в масле 2,5% 1 мг, отменить Тромбо-Асс/АспиринКардио и Фраксипарин/Клексан.
При коричневой мазне: Но-шпа 2т/ до 3 р. и свеча Папаверин.
При коричнево-кровянистой мазне: уколоть 1 мл 2,5 % Прогестерона в масле (ампулу перед уколом необходимо нагреть до 30-40 градусов, и растереть полупопие до красноты), пить Дицинон - 3-4 табл. в день.
При алых выделениях: укол Прогестерона и укол Дицинона в/м 2 мл (до 4 уколов в день),
укол Но-шпы - 3 раза в день, Транексам - 1т.*3р./день до чистого дня.
При отслойке: Транексам в/м 2 мл 2-3 раза в день.
Помогает и Метацин, который, к сожалению, продается преимущественно по рецепту. Обычно его назначают по 1 таблетке 3 раза в день (когда сохраняют), или по 1 таблетке при болях.
Если есть физическая и финансовая возможность - вызывайте скорую и госпитализируйтесь. Ваша беременность, которую вы так долго ждали, не повод для рисков. Лучше перестраховаться!
Приметы, ритуалы и просто отвлекалочки
1. На пункцию и перенос одеваем красные труселя, красные тапочки и красную рубашку-футболку! Опрос показал, что почти всегда эта примета работает.
2. Перед протоколом выбросить или отдать подругам ВСЕ прокладки и тампоны!!!
3. Написать на бумажке слова "Моя беременность! Хранить 9 месяцев", взять презерватив, засунуть бумажку и завязать, запихнуть опять в упаковку и скрепить степлером, спрятать куда-нить в укромное место, где никто не найдет и забыть до родов)))
4. Взять большую скрепку (мама) и маленькую скрепку (ребенок), скрепить, спрятать туда же.
5. Купить соску - положить под матрас.
6. Две рыбки под матрас (н-р, конверт с карпиками в магазине фен-шуй).
7. Куклу на Запад посадить.
8. Купить тест на беременность. Подходишь к аптекарше и говоришь так серьезно "Дайте мне, пожалуйста, положительный тест". Нарисовать красным фломастером полосочку, старайся чуть выше предполагаемой беременной. Когда время придет тестироваться, используй только ЭТОТ тест.
9. Собирай что-нить в полосочку.
10. Прямо с сегодняшнего дня отменить все свои болезни. Просто приказать своему телу не болеть и поставить диагноз - ЗДОРОВА!
11. На баночке с витаминами, с любым лекарством прилепить наклейку со словом "Заберемениватель".
А главное - верить в себя!!!
Признаки беременности
Отделить признаки беременности от последствий пункции и приема препаратов стимуляции и поддержки довольно проблемно.
Все признаки беременности в организме появляются на фоне растущего ХГЧ и гормонов это происходит обычно не ранее 14-20 ДПП.
По нашему опыту признаков беременности на ранних сроках может не быть никаких. Большинство наших ощущений можно объяснить принимаемыми препаратами и последствием пункции яичников:
- Прегнил (ХГЧ) от пункции сохраняется в организме еще неделю после подсадки и вызывает большинство признаков: набухание груди, частое мочеиспускание, вздутие кишечника, боли в матке, сонливость, повышенный аппетит, склерозность, тошноту.
Поэтому на 6-7ДПП, если нет прегнила в поддержке все эти признаки спадают и появляется чувство «провала». В это время свой ХГЧ еще мал и не чувствуется. А вот все то же на 12-14ДПП уже свидетельствуют о росте ХГЧ своего.
Прогинова/Дивигель, Дюфастон/Утрожестан/Прогестерон тоже «виноваты» в болезненности груди и вздутии живота, повышенной температуре тела (до 37.4) и в остальных признаках.
Боли в тазу и спине, тянущие боли в матке могут быть следствием пункции.
Часто имплантация происходит совершенно незаметно, иногда сопровождается покалыванием в матке, прострелами от пупка в ногу и пр.
Поэтому не имеет смысла переживать, если у вас все тихо и спокойно, а просто ждать.
Примеры ХГЧ:
Если у вас в поддержке есть Прегнил (или аналог) сдавать ХГЧ раньше 14ДПП не имеет смысла, так как прегнил выводится долго. ХГЧ менее 40 ед на 14ДПП часто оказывался следом Прегнила. Результаты разных лабораторий могут отличаться!
Если у вас нет Прегнила, то пробовать сдать ХГЧ можно не ранее 8-9ДПП, были случаи, когда на 8 ДПП ХГЧ 1.2 ед, а на 10 ДПП - 30!!! И в любом случае пересдать на 14ДПП.
ХГЧ появляется в крови на следующий день после имплантации и удваивается каждые 48-72 часа. В моче концентрация ХГЧ в 2-3 раза слабее, чем в крови, поэтому тесты могут не показать полоски даже на 14 ДПП!!! Часто такое происходит у тех, кто имеет проблемы с почками (недостаточность). Делать тест надо утром после 5-7 часового воздержания от мочеиспускания! Тест должен иметь чувствительность 10-20 мЕ (Эви тест), Фрау тест имеет чувствительность 25 ед и часто вредничает.
Если эмбриона два - ХГЧ удваивается. Имплантация 2-3-дневных эмбрионов происходит обычно на 3-8ДПП (бывает и позднее), 5-дневных эмбрионов на 1-4ДПП.
ХГЧ на 14ДПП в среднем от 70 до 700 ед для одного малыша. Вне зависимости от начальной цифры, малыши развиваются нормально! Большая цифра ХГЧ на 8-10ДПП и полоски на тесте с 6 ДПП могут говорить о двойне. Часто бывает замирание одного из эмбрионов, тогда ХГЧ перестает пропорционально расти, что может вас напугать. Как правило, начинаются выделения из-за отслоения замершего эмбриона., что не сказывается на другом ПЯ.
Анализ на ХГЧ
можно сдать:
Новые Медицинские технологии. Самый быстрый экспресс анализ за 1 час (доплата за срочность 200 руб. - оно того стоит).
1.ул. Мечникова, 144, +7 (863) 290-31-55
2.ул. Социалистическая, 74, +7 (863) 200-30-73
3.ул. Краснодарская 2-я, 147/3, +7 (918) 583-10-61
4.Днепровский пер., 122/1, +7 (863) 298-02-99
Евродон
1.ул. Вавилова, 57
2.ул. Социалистическая, 208.
Срок исполнения 2 часа.
НИИАП
Ул. Мечникова, 43
Обращаться в окошко «Платные услуги» - там дешевле. Срок исполнения 3-4 часа.
НАУКА
1. ул. Социалистическая, 167
2. ул. Тургеневская, 49
3. Коммунистический просп., 10а
4. просп. Стачки, 194, корп.1, оф. 209.
Вспомогательные репродуктивные технологии (ВРТ) продолжают активно развиваться и становятся частью рутинного подхода к решению проблемы деторождения. Количество детей, рожденных благодаря этим технологиям в Европе, по данным на 2008 год, составило 4,2%. Тем не менее, несмотря на первоначальные существенные положительные сдвиги в результатах и понимании процесса ВРТ, уровень живорождения благодаря данным технологиям на каком-то этапе своего развития остановился, и с недавних пор
Девочки нашла тут статью, хочу поделиться. Если б в свое время я была бы более внимательной к таким вещами (не говорю о врачах) ЭТОГО можно было бы избежать  Тромботические осложнения являются наиболее серьезными, потенциально смертельными осложнениями вспомогательных репродуктивных технологий. Частота использования искусственных репродуктивных технологий продолжает активно увеличивает, так в 2004 году в Европе эти методики были применены более чем у 250 000 женщин [1]. У женщин, включаемых в программы ЭКО, имеет место объективно более высокий риск венозных тромбоэмболических осложнений (ВТЭ). Это связано с их более старшим возрастом, высокой распространенность метаболического синдрома и сопутствующей патологии. Нельзя также не учитывать четкую взаимосвязь между бесплодием и тромбофилическими состояниями, как генетически обусловленными, так и приобретенными, включая антифосфолипидный синдром (АФС). Несмотря на то, что частота ВТЭ у этой группы пациенток согласно мировым данным невысока (0,08-0,11%) [2], учитывая тяжелые осложнения ВТЭ, в том числе и фатальные, а также повышенный риск ВТЭ у пациенток, включаемых в программы ЭКО, этот вопрос требует особого внимания.
Тромботические осложнения являются наиболее серьезными, потенциально смертельными осложнениями вспомогательных репродуктивных технологий. Частота использования искусственных репродуктивных технологий продолжает активно увеличивает, так в 2004 году в Европе эти методики были применены более чем у 250 000 женщин [1]. У женщин, включаемых в программы ЭКО, имеет место объективно более высокий риск венозных тромбоэмболических осложнений (ВТЭ). Это связано с их более старшим возрастом, высокой распространенность метаболического синдрома и сопутствующей патологии. Нельзя также не учитывать четкую взаимосвязь между бесплодием и тромбофилическими состояниями, как генетически обусловленными, так и приобретенными, включая антифосфолипидный синдром (АФС). Несмотря на то, что частота ВТЭ у этой группы пациенток согласно мировым данным невысока (0,08-0,11%) [2], учитывая тяжелые осложнения ВТЭ, в том числе и фатальные, а также повышенный риск ВТЭ у пациенток, включаемых в программы ЭКО, этот вопрос требует особого внимания.
Изменения гемостаза, связанные со стимуляцией овуляции
Стимуляция овуляция приводит к возникновению состояния гиперэстрогении. При этом, как и в случае применения оральных контрацептивов и препаратов заместительной гормональной терапии, в результате воздействия экзогенных эстрогенов формируется состояние гиперкоагуляции. Исследования, посвященные изучению влияния сверхфизиологических уровней эстрогенов на систему гемостаза, очень ограничены. Кроме того, интерпретация их результатов осложняется использованием различных протоколов стимуляции овуляции, а также тем, что в эти исследование было включено очень небольшое количество пациенток. В целом результаты этих исследований свидетельствуют о том, что уровни эстрадиола коррелируют с концентрацией фибриногена, уровнями D-димера и резистентностью к АРС [3]. Кроме того, стимуляция овуляции также ассоциируется с увеличением уровней некоторых факторов свертывания крови: фактора V, фибриногена, фактора Фон Виллебранда. Одновременно выявляется повышение маркеров активации система гемостаза - фрагментов протромбина F 1+2 и D-димера и нарушение функций эндогенной антикоагулянтной системы, что проявляется снижением уровней антитромбина и протеина S. Резистентность к АРС увеличивает при стимуляции овуляции и сохраняется на повышенном уровне при проведении поддержки лютеиновой фазы. Важно отметить, что нарушение функции естественных антикоагулянтов и развитие резистентности к АРС представляет особый риск у пациенток с мутацией FV Leiden и антифосфолипидным синдром, когда уже исходно имеющаяся резистентность к АРС определяется фоновое повышение риска тромбоэмболических осложнений.
В еще большей степени эти изменения гемостаза развиваются при синдроме гиперстимуляции яичников (СГЯ). СГЯ сопровождается повышением уровней фибриногена, D-димера, комплексов тромбин-антитромбин и F1+2, снижением уровня прекалликреина и тканевого фактора [4], причем эти изменения сохраняются в течение нескольких недель. Интересно, что повышенные уровни D-димера и комплексов тромбин-антитромбин ассоциируется с неудачами ЭКО [3]. Подобная взаимосвязь между избыточной активацией коагуляции и неудачными результатами ЭКО еще раз подтверждает важность механизмов гемостаза в процессе имплантации. В отличие от нормальных циклов стимуляции овуляции, когда наблюдаются минимальные изменения гематокрита, при СГЯ имеет место выраженная гемоконцентрация, что многократно повышает риск ВТЭ.
Следует обратить внимание на то, что клиническая картина ВТЭ при стимуляции овуляции редко развивается до введения хорионического гонадотропина (ЧХГ). Это наблюдение поставило перед учеными вопрос о роли ЧХГ для активации системы гемостаза. Было показано, что после назначения ЧХГ происходит повышение уровней фибриногена, факторов II, V, VII, VIII и IX. Вслед за такой активацией прокоагулянтных механизмов с задержкой на 2 дня запускаются фибринолитические механизмы, пик активности которых достигает через 8 дней [4]. Кроме того, при использовании очищенного ФСГ мочевого происхождения, которые также содержат ЧХГ, наблюдается снижение уровней протеина С и антитромбина, в то время как для рекомбинантного ФСГ эти изменения не были статистически достоверными по сравнению с женщинами с нормальным менструальным циклом [5]. Таким образом, гиперкоагуляция, связанная с гиперэстрогенией, имеющая место во время стимуляции овуляции, может усиливаться под действием ЧХГ, что имеет место и во время физиологической беременности.
В большинстве случаев для развития тромбоза требуется «синнергичный» эффект нескольких факторов риска (табл. 1).
Таблица 1.
Патогенез тромботических осложнений в условиях стимуляции овуляции и СГЯ
| Гемоконцентрация
Сдавление тазовых вен Состояние гиперкоагуляции Тромбофилические состояния Личный или семейный анамнез тромботических осложнений Нарушение реактивности сосудов |
Риск тромбоэмболических осложнений при использовании вспомогательных репродуктивных технологий
Несмотря на описанные выше выраженные изменения гемостаза, которые возникают при использовании вспомогательных репродуктивных технологий, общая частота ВТЭ в абсолютных значениях остается не высокой. В целом риск ВТЭ у женщин, включенных в программы ЭКО, в 10 раз превышает риск ВТЭ у женщин репродуктивного возраста, который составляет 2-3 на 10 000 человек в год. В то же время при наличии СГЯ тромбоэмболические осложнения развиваются у одной из 128 женщин, таким образом, риск ВТЭ по сравнению с общей популяцией возрастает в 20-40 раз [6]. Согласно недавнему обзору Nelson S.M. и соавт. (2008), при литературном поиске авторам удалось идентифицировать 109 описанных случаев тромбоэмболических осложнений, связанных с использованием вспомогательных репродуктивных технологий [1]. В 70% имели место венозные тромбоэмболические осложнения. Интересно, что в отличие от наиболее часто развивающихся во время беременности илиофеморальных тромбозов, у этих пациентов преобладали тромбозы глубоких вен верхних конечностей, включая тромбозы подключичной и внутренней яремной вены. В качестве одного из возможных патофизиологических механизмов этого явления считают особенности дренирования перитонеальной жидкости, содержащей высокие уровни эстрогенов, в грудной лимфатический проток. В этом случае, вероятно, роль играет сочетание нескольких факторов: анатомических особенностей, состояния гиперкоагуляции, обусловленного экзогенными факторами, и наличие тромбофилий. В 30% случаев тромбозы развиваются у женщин, у которых беременность не наступила. Более того, время до развития тромбоза оказалось больше, чем было принято считать ранее. В среднем тромбоэмболические осложнения развиваются через 40 дней после переноса эмбриона и через 27 дней после индукции овуляции [2]. Описаны случаи тромбозов на фоне стимуляции овуляции в лютеиновую фазу, а также отсроченные тромботические осложнения через 6-7 недель после овуляции. У женщин с СГЯ тромбоэмболические осложнения развивались от нескольких дней до нескольких недель после разрешения симптомов. Более того, описан случай тромбоза после ЭКО на 20-й неделе беременности. Все это свидетельствует о длительной персистенции генерализованных изменений в системе гемостаза в сторону гиперкоагуляции на фоне стимуляции овуляции, о чем нужно всегда помнить при выработке тактики профилактики тромбозов у женщин, вступающих в программу ЭКО.
Артериальные тромбозы у пациенток, включенные в программы ЭКО, развиваются реже, чем венозные, и в более короткие сроки: в среднем через 10-14 дней после переноса эмбриона.
Роль тромбофилии в патогенезе тромботических осложнений программ вспомогательных репродуктивных технологий
Важно помнить о том, что тромбоэмболические осложнения могут развиваться и при отсутствии тяжелого СГЯ, сопровождающегося гемоконцентрацией. По данным Delvigne А. и соавт. (2004), у пациенток с тромбозами в 12% имел место СГЯ средней тяжести и примерно у такого же процента пациенток - СГЯ легкой степени [7]. Кроме того, тяжелые формы СГЯ выявляются у 0,56-6,5% женщин с СГЯ, тогда как тромботические осложнения развиваются у 1 из 128 женщин с СГЯ. Таким образом, для развития тромбозов значение могут иметь и другие фоновые факторы риска тромботических осложнений, в частности, наследственная и приобретенная тромбофилия. Наследственная тромбофилия была выявлена у 23% женщин с СГЯ, причем в 18% обнаружена мутация FVLeiden [8]. Dulitzkyи соавт. (2002) провели проспективную оценку маркеров тромбофилии, включая плазменные уровни антитромбина III, протеина S, протеина С, антифосфолипидных антител, мутацию FVLeiden и MTHFRC677T, у пациенток, госпитализированных в связи с тяжелым СГЯ. При этом один или более маркеров тромбофилии были положительными у 85% женщин. В контрольной группе ни в одном случае не было обнаружено более одного маркера тромбофилии, а частота выявления одного маркера составила 27% [9]. Кроме того, описаны случаи тромботических осложнений на фоне стимуляции овуляции у пациенток с отягощенным семейным анамнезом по тромбозам, при этом известные тромбофилии выявлены не были. Это может свидетельствовать о роли еще не изученных наследственных нарушений в системе гемостаза в патогенезе тромбозов, связанных с использованием вспомогательных репродуктивных технологий. В связи с этим при планировании стимуляции овуляции и стратегий профилактики тромботических осложнений особое внимание необходимо уделять оценке личного и семейного тромботического анамнеза.
Оценка факторов риска тромботических осложнений перед использованием вспомогательных репродуктивных технологий
Перед включением пациенток в программы вспомогательных репродуктивных технологий необходима индивидуальная оценка факторов риска, включая наличие тромбофилических состояний, отягощенного семейного и личного тромботического анамнеза, индекса массы тела, сопутствующих заболеваний, возраста (> 40 лет). Важно отметить, что многократные неудачи ЭКО ассоциируются с высокой частотой тромбофилий, таким образом, эти пациентки относятся к группе повышенного риска по развитию тромбоэмболических осложнений. Так, высокая частота мутаций FV Leiden, протромбина G20210А, MTHFR C677T была с более высокой частотой выявлена у женщин с тремя и более неудачами ЭКО по сравнению с женщинами, забеременевшими с первой попытки, или женщинами, у которых беременность наступила спонтанно [10]. Таким образом, пациенты из этой группы могут быть подвержены значительно более высокому риску развития тромбоэмболических осложнений. У таких женщин мы настоятельно рекомендуем проводить обследование на наличие наследственных и приобретенных форм гемостаза. Это позволяет нам уже на этапе фертильных циклов начать патогенетически обоснованную профилактику с применением низкомолекулярного гепарина, обеспечивающую создание оптимальных условий для имплантации и профилактику тромботических осложнений. Особое внимание следует обратить на высокую частоту антифосфолипидного синдрома у пациенток, включенных в программы вспомогательных репродуктивных технологий, которая составляет 10-48% по сравнению с 1-5% в общей популяции [1]. У таких пациенток повышен риск неудач ЭКО, нарушений имплантации и тромбоэмболических осложнений. Наличие генетических форм тромбофилий, особенно их сочетание с антифосфолипидным синдромом, однонаправленность действия различных форм тромбофилии могут быть причиной клинически не диагностированных ранних преэмбрионических потерь. Антифосфолипидные антитела повышают экспрессию ингибитора активатора плазминогена 1 (PAI-1) и тканевого фактора, что усиливает протромботические механизмы и снижает активность фибринолиза, приводя к дефектам имплантации и снижению глубины децидуальной инвазии трофобласта.
Если считать тромбофилию постоянно персистирующим фактором у женщин с генетической тромбофилией или АФС, то первые ее эффекты представляются как дефекты имплантации плодного яйца, недостаточная глубина инвазии трофобласта, неполноценная плацентация и, как следствие, эндотелиопатия. Предполагается возможная этиологическая роль АФА в генезе бесплодия и привычного выкидыша, препятствующих развитию цитотрофобласта в синцитиотрофобласт на ранних сроках беременности. С нашей точки зрения, новая эра в понимании этиологии и патогенеза бесплодия и неудач ЭКО (в том числе преэмбрионических потерь беременности - после ЭКО) началась с открытия новых наиболее часто встречающихся в общей популяции генетических дефектов гемостаза тромбофилического характера и АФС, а также с установления роли тромбофилии в патологии процессов имплантации плодного яйца, плацентации и более поздних нарушениях маточно-плацентарной перфузии. В процессе подготовки к имплантации под влиянием прогестерона в эндометрии происходит повышение содержания PAI-1, тканевого фактора и снижение уровня активаторов плазминогена тканевого и урокиназного типов, металлопротеаз матрикса и вазоконстриктора - эндотелина 1. Эти физиологические механизмы регуляции гемостаза, фибринолиза, экстрацеллюлярного матрикса и сосудистого тонуса направлены на предотвращение образования геморрагии при дальнейшей инвазии трофобласта. Со своей стороны бластоциста синтезирует активаторы плазминогена тканевого и урокиназного типов и протеазы, которые необходимы для разрушения экстрацеллюлярного матрикса в процессе имплантации. Их излишний синтез в свою очередь регулируется хорионическим гонадотропином. В процессе «дозированного» разрушения матрикса под действием ферментов, выделяемых бластоцистой, клетки эндометрия, которые содержат определенное количество экстраваскулярного фибрина, не фагоцитируются, а как бы «отодвигаются» посредством «контактного ингибирования». Эта фаза процесса имплантации носит название «аваскулярной», или «гистиотрофной». Следует отметить, что это наиболее уязвимая фаза имплантации: часто такие факторы, как вирусы, токсины, антитела и пр., могут непосредственно влиять на полноценность имплантации. С точки зрения влияния тромбофилии наиболее ярким примером являются полиморфизм-1 и другие генетически обусловленные дефекты фибринолиза с повышением уровня PAI-1, гиперфибриногенемией и АФА. Так, согласно нашим данным, тромбофилия как сложный интегральный (с нашей точки зрения, и инициальный) фактор неудачи ЭКО была обнаружена у 90% пациенток с неудачами ЭКО в анамнезе [11]. Таким образом, подготовка к ЭКО женщин с бесплодием и тромбофилией требует особого похода.
В большинстве случаев возникновение тромбозов связано с синдромом гиперстимуляции яичников (СГЯ), поэтому этому серьезному осложнению мы решили посвятить отдельный раздел.
Синдром гиперстимуляции яичников
СГЯ является жизнеугрожающим состоянием, симптомы которого колеблются от легкого недомогания до развития ОРДС, почечной недостаточности и тромбозов. При ЭКО СГЯ развивается у 1-10% женщин. Тромбоэмболические осложнения при СГЯ развивается в 0,04% случаев [12].
Факторами риска развития СГЯ являются молодой возраст пациентки, низкий вес, наличие синдрома поликистозных яичников. Считается, что у женщин молодого возраста плотность рецепторов гонадотропинов больше, следовательно, больше и чувствительность к ним. У пациентов к СГЯ с достоверно большей частотой выявляются атопии по сравнению с контрольной группы [13]. Возможно, нарушение иммунологических механизмов приводит к развитию гиперчувствительности и воспалительного ответа даже в ответ на неспецифические стимуляторы. Риск развития СГЯ во многом определяется видом программы ЭКО. Риск СГЯ больше при применении агонистов гонадолиберин-рилизинг гормона, чем при применении его антагонистов [14]. Еще меньше риск развития СГЯ при применении кломифена цитрата или менопаузального хорионического гонадотропина. Факторами риска СГЯ также является стремительное увеличение уровня эстрадиола в плазме крови (>2500 пг/мл), появление множества фолликулов среднего размера по данным ультразвукового исследования. Кроме того, если в результате ЭКО наступает беременность, начинается дополнительная выработка эндогенного ХГЧ, что увеличивает риск развития СГЯ. Факторы риска развития СГЯ суммированы в табл. 2.
Таблица 2.
Факторы риска развития СГЯ
| Характеристика пациентки:
Молодой возраст (<30 лет) Низкая масса тела СГЯ в анамнезе Сидром поликистозных яичников Использование высоких доз гонадотропинов для стимуляции овуляции Применение ХГЧ, а не прогестерона для поддержки лютеиновой фазы Большое количество антральных в яичнике, по данным УЗИ, до начала стимуляции овуляции Быстрый рост концентрации эстрадиола (>2500 пг/мл) Большое число полученных ооцитов (>20) Наступление беременности |
Описаны семейные случаи СГЯ, в том числе и рецидивов этого синдрома и его развитие во время беременности у родственников. Это может свидетельствовать о наличии наследственных признаков, определяющих повышенный риск развития этого синдрома. Так, сообщается об обнаружении у пациенток с СГЯ полиморфизма рецепторов ФСГ, которые определяют повышенную чувствительность рецепторов к этому гормону [12].
Патогенез СГЯ
Репродуктивные технологии включают применение антагонистов или агонистов гонадолиберин-рилизинг гормона для стимуляции яичников и человеческого хорионического гонадотропина (ХГЧ) для индукции овуляции. Стимуляция яичников может приводить к их избыточной активации и развитию СГЯ. Развитие этого синдрома связывают с применением экзогенного ХГЧ. Крайне редко СГЯ может возникать при самопроизвольной беременности (чаще в условиях, когда наблюдается повышенная продукция ХГЧ, например, при многоплодной беременности), а также при стимуляции овуляции кломифеном цитратом [8]. Основным характерным признаком, обнаруживающимся при СГЯ, является двустороннее увеличение яичников за счет множественных кист. При морфологическом исследовании в таких яичниках выявляются многочисленные желтые тела, фолликулярные кисты и выраженный отек овариальной стромы. Образование кист в яичниках при СГЯ предположительно связано с непосредственным влиянием стимуляции гонадотропинами, так как сходные изменения в яичниках наблюдаются и при других состояниях, сопровождающихся повышенными уровнями эндогенных гонадотропинов, например, при пузырном заносе, хорионкарциноме и многоплодной беременности.
Патогенез СГЯ пока еще мало изучен. Предполагается, что при СГЯ происходит выброс из яичника вазоактивных субстанций (цитокины, ангиотензин, эндотелиальный сосудистый фактор роста). Это приводит к повышению проницаемости сосудов и выходу белков и жидкости в интерстициальное пространство. В результате развивается асцит, гидроторакс, анасарка, гемоконцентрация и тромбоэмболические осложнения. При СГЯ происходит падение артериального давление, увеличение сердечного выброса, активация ренин-ангиотензин-альдостероновой и симпатоадреналовой системы.
Весьма интересна история развития представлений о патогенезе СГЯ. Впервые подтверждения того, что основным механизмом патогенеза СГЯ является повышение проницаемости капилляров, выло показано в экспериментах на кроликах с использованием внутривенного красителя [15]. При этом основным условием для перехода жидкости из внутрисосудистого пространства в брюшную полость было наличие яичников. СГЯ в экспериментах не удалось индуцировать ни у животных мужского пола, ни у мужчин. Эти эксперименты легли в основу концепции о том, что ключевым фактором для развития СГЯ является наличие яичников, которые секретируют вазоактивный медиатор. Кроме того, позднее при СГЯ был выявлен феномен активации ангиогенеза. В дальнейшем многочисленные эксперименты были направлены на то, чтобы установить этот медиатор, выделяемый яичниками и повышающий проницаемость сосудов. Исходно внимание ученых было обращено к изучению эстрогенов, прогестнинов и пролактина в качестве медиаторов СГЯ, однако прямое патогенетическое значение этих субстанций для развития СГЯ выявить не удалось. Так, развитие асцита у кроликов женского пола не было связано с высокими дозами эстрогенов и прогестерона [7]. Таким образом, повышенный уровень эстрадиола служит маркером ответа яичников на стимуляцию, но не является причиной для возникновения СГЯ.
Доказанным фактом является то, что ренин-ангиотензин-альдостероновая система (РААС) принимает активное участие в механизмах развития СГЯ. С одной стороны, яичники секретируют некоторые компоненты РААС, с другой, на функционирование РААС оказывает непосредственное влияние ХГЧ, который напрямую ассоциирован с СГЯ. Также была подтверждена системная активация РААС в условиях гемодинамических сдвигов у пациенток с СГЯ. Однако остается неясным, могут ли компоненты РААС быть основным патогенетическим звеном СГЯ или эта система активируется вторично в качестве ответа организма на гиповолемию в условиях СГЯ,
Патофизиологические изменения, происходящие в условиях СГЯ, напоминают агрессивно развивающийся системный воспалительный ответ. Однако данные о роли цитокинов в патогенезе СГЯ весьма противоречивы. Эти низкомолекулярные протеины проявляют свою активность в крайне низких концентрациях и реализуют свои эффекты при помощи аутокринных, паракринных и эндокринных механизмов. На активность цитокинов оказывает влияние функциональный статус цитокиновых рецепторов, наличие ингибиторов цитокинов, растворимых рецепторов и связывающих белков. Тем не менее большинство исследований в этой области указывает на повышение уровней медиаторов ранней фазы воспаления (ИЛ-1, ИЛ-2, ИЛ-6, ИЛ-18, ИЛ-18, TNF-альфа и сосудистого эндотелиального фактора роста) и на одновременное снижение уровней иммуносупрессивных и противовоспалительных цитокинов (ИЛ-10) на ранних стадиях развития СГЯ. Существует гипотеза о врожденных дефектах иммунного ответа, обуславливающих повышенный риск СГЯ. Растворимая молекула адгезии клеток сосудов-1 (sVCAM-1) и растворимая молекула межклеточной адгезии-1 (sICAM-1), которые принадлежат к суперсемейству иммуноглобулинов и являются основными медиаторами адгезии лейкоцитов, их взаимодействий с сосудистой стенкой и экстравазации в процессе иммунных и воспалительных реакций, также могут участвовать в патогенезе СГЯ. Это предположение было доказано в одном из исследований по типу случай-контроль по оценке уровней sICAM-1 и sVCAM-1 в перитонеальной жидкости и в плазме крови [16]. Еще в одном исследовании в сыворотке крови и в асцитической жидкости у пациенток с СГЯ были выявлены более высокие уровни sICAM-1 и более низкие уровни растворимого Е-селектина - еще одной молекулы, контролирующей эндотелиальную адгезию [16]. Конкретные механизмы участия этих медиаторов в патогенезе СГЯ еще предстоит установить, однако на данном этапе ясно, что они имеют значение для регуляции сосудистой проницаемости.
Повышение сосудистой проницаемости с последующим развитием асцита при СГЯ связано с субстанциями, накапливающимися в фолликулярной жидкости. Одним из важнейших таких факторов, принимающих участие в патогенезе СГЯ, предположительно является VEGF. Существует несколько доказательств этой гипотезы. Во-первых, уровни VEGF в фолликулярной жидкости превышают таковые в плазме крови. Во-вторых, во время овуляции регистрируется повышение концентрации VEGF в крови. Кроме того, введение ХГЧ стимулирует экспрессию мРНК VEGF лютеинизирующимися клетками гранулезы яичников [17], что объясняет, почему введение ХГЧ часто является критическим фактором для развития СГЯ. Повышенные уровни VEGFв плазме крови и перитонеальной жидкости были выявлены у пациенток с СГЯ по сравнению с контрольной группой [18]. Усиленная экспрессия мРНК VEGF была описана у пациенток с синдромом поликистозных яичников, для которых характерен повышенный риск развития СГЯ. Тем не менее конкретные патогенетические механизмы, посредством которых VEGF обуславливает развитие СГЯ, остаются не до конца известными.
Большой вклад в изучение роли VEGF в патогенезе СГЯ внес Rizk и соавт. (1997) [19]. VEGF представляет собой член семейства гепарин-связывающих протеинов, который непосредственно воздействуют на эндотелиальные клетки и индуцирует процессы пролиферации и ангиогенеза. VEGF кодируется общим геном с фактором сосудистой проницаемости (VPF), которые способствует экстравазации белков в сосудах злокачественных опухолей. В результате транскрипции этого гена при участии альтернативного сплайсинга получаются несколько изоформ VEGF. Семейство VEGF включает четыре разных димерных формы (A-D) и плацентарный фактор роста. Все члены семейства VEGF связываются с тремя рецепторами (VEGF-R 1-3), которые экспрессируются на эндотелиальных клетках. Было идентифицировано и клонировано два рецептора VEGF (VEGFR-1 и VEGFR-2), которые относятся к семейству тирозинкиназных рецепторов. VEGFR-1 экспрессируется на эндотелиальных клетках, клетках трофобласта, моноцитах и мезангиальных клетках в почках. VEGFR-2 также экспрессируется на гемопоэтических стволовых клетках и мегакариоцитах. Экспрессия VEGF стимулируется под действием гипоксии, а также цитокинами и простагландинами. Таким образом, цитокины и факторы роста, непосредственно не стимулирующие ангиогенез, могут модулировать процессы ангиогенеза путем влияния на экспрессию VEGF. Иными словами цитокины могут оказывать непрямой ангиогенный и антиангиогенный эффект. Продукцию VEGF стимулирует трансформирующий фактор роста бета, фактор роста фибробластов-4, фактор роста тромбоцитарного происхождения, инсулиноподобный фактор роста, интерлейкин-1бета и интерлейкин-6, тогда как тромбоспондин и интерлейкин-10 подавляют экспрессию VEGF. VEGF синтезируется и депонируется в гранулах Т-лимфоцитов, тучных клеток, нейтрофилов и мегакариоцитов. VEGF-А или собственно VEGF существует минимум в 5 изоформах, имеющих разную молекулярную массу. Главное, что отличает эти изоформы друг от друга, это способность к связыванию гепарина и гепарин-сульфата.
InvivoVEGF является мощным медиатором сосудистой проницаемости. Он также принимает непосредственное участие в инициации и поддержании ангиогенеза на различных этапах эмбриогенеза, а также в тканях взрослого организма, для которых характерны интенсивные процессы новообразования сосудов, например, в ткани эндометрия и лютеинизирующихся фолликулах. Помимо своей физиологической роли VEGF выполняет свои функции и в условиях патологии, являясь критически важным фактором ангиогенеза при становлении васкуляризации опухолей. Повышенные уровни VEGF также выявляются в перитонеальной жидкости в условиях эндометриоза. VEGF может играть важную роль в регуляции циклических процессов ангиогенеза в яичниках, а его способность повышать сосудистую проницаемость может служить важным фактором для обеспечения продукции секрета маточных труб и появления фолликулярной жидкости, а также жидкости в доброкачественных опухолях яичника, имеющих эпителиальную выстилку, которая содержит VEGF. GordonJD и соавт. (1996) показали, что VEGF в здоровых яичниках локализуется в слое тека-клеток, тогда как содержание этого белка в клетках гранулезы минимальное. VEGF не экспрессируется в атрезирующихся фолликулах и дегенерирующем желтом теле [20]. В то же время высокий уровень VEGF обнаруживается в хорошо васкуляризованном желтом теле. В постменопаузе в яичниках VEGF в норме не выявляется и обнаруживается только в инклюзионных эпителиальных кистах и серозных цистаденомах. На основании этих экспериментальных данных авторы сделали вывод о том, что в течение репродуктивного периода VEGF играет важную роль для процессов роста и поддержания функции фолликулов и желтых тел в яичнике, что осуществляется на уровне модуляции ангиогенеза.
Молекулярно-биологические исследования свидетельствуют о четкой взаимосвязи между VEGF и ХГЧ [19]. Было показано, что экспрессия мРНК VEGF у крыс и в яичниках приматов происходит преимущественно после пика ЛГ. Этот пик ЛГ также является ключевым фактором и для развития СГЯ. Кроме того, использование антагониста ГнРГ в лютеиновую фазу с целью подавления выброса ЛГ приводит к торможению экспрессии мРНК VEGF. Отсюда ясно, почему использование прогестерона для поддержки лютеиновой фазы снижает вероятность развития СГЯ по сравнению с ХГЧ. Экспрессия VEGF под влиянием ХГЧ в яичниках осуществляется в клетках гранулезы и зависит от его дозы. Активность VEGF нарастает в процессе роста граафова фолликула и достигает пика при формировании желтого тела [21]. Было показано, что именно повышенная суммарная продукция VEGF на уровне фолликулов обуславливает нарастание уровней VEGF в плазме крови, что ассоциируется с развитием СГЯ [22].
Фактор фон Виллебранда (vWF) считается маркером активации эндотелиальных клеток. Его концентрация повышается в условиях избыточной экспрессии VEGF эндотелиальными клетками. Было показано, что повышенные уровни vWF в день переноса эмбрионов коррелируют с тяжестью СГЯ, а повышение уровней vWF предшествует развитию тяжелого СГЯ [23]. Однако такого повышения уровней vWF не было зарегистрировано в фолликулярной жидкости, что указывает на то, что повышенные уровни vWF не могут быть яичникового происхождения. По всей видимости, источником vWF при СГЯ является эндотелий, а на выброс vWF оказывают вазоактивные медиаторы овариального происхождения. У пациенток с СГЯ по сравнению с женщинами с высоким ответом на стимуляцию было выявлено более выраженное повышение уровней vWF за день до забора ооцитов, причем повышенные уровни vWF сохранялись в условиях СГЯ в течение всей лютеиновой фазы, тога как у пациенток без СГЯ уровни vWF прогрессивно снижались после забора ооцитов [24]. Снижение уровней vWF при СГЯ сопровождает клиническое улучшение. Таким образом, в клинической практике повышенные уровни vWF можно рассматривать в качестве прогностических для развития СГЯ и в качестве дискриминаторного параметра. Однако vWF предположительно играет роль в генезе формирования патологического каскада реакций в условиях СГЯ в качестве вторичного медиатора, который выделяется эндотелиальными клетками в ответ на их стимуляцию фактором яичникового происхождения.
Вазоконстриктор эндотелин-1 является еще одном фактором, повышающим сосудистую проницаемость. При СГЯ его концентрация в фолликулярной жидкости в 100-300 раз превышает таковую в плазме крови. У пациенток с СГЯ выявляется повышение плазменных уровней эндотелина-1, однако его концентрации нарастают параллельно с содержанием в крови других нейрогуморальных вазоактивных факторов и коррелируют с тяжестью СГЯ [25], что может говорить о том, что повышение уровней эндотелин-1 является частью ответа организма, направленного на сохранение гомеостаза, а не инициирующим фактором в развитии СГЯ.
Роль эндотелия в патогенезе СГЯ. Впервые роль эндотелия в патогенезе СГЯ была показана в элегантном исследовании Albert С. и соавт. (2002) [18]. В основу этой гипотезы легли более ранние наблюдения о более высоком уровне VEGF в плазме крови по сравнению с фолликулярной жидкостью у женщин из группы риска развития СГЯ [26]. Это свидетельствует о том, что другие клетки помимо фолликулярных могут быть источником и мишенями для VEGF. Для тестирования этой гипотезы Albert С. и соавт. создали invitro модель, в которой проверяли воздействие эстадиола и ХГЧ на человеческий микрососудистый эндотелий с целью оценки способности эндотелиальных клеток к экспрессии и секреции медиаторов, которые могут быть вовлечены в патогенез СГЯ [18]. В результате этих экспериментов было показано, что эндотелий является источником VEGF и ИЛ-6. Эти медиаторы могут реализовывать свое воздействие на паракринном и аутокринном уровне, индуцируя изменения в сосудах, связанные с СГЯ, Рецепторы к VEGF и ИЛ-6 были обнаружены в клетках желтого тела. Кроме того, была установлена роль этих рецепторов для повышения сосудистой проницаемости у человека [27]. Albert С. и соавт. в своем исследовании установили, что ХГЧ индуцирует экспрессию KDR в эндотелиальных клетках человека - наиболее функционального рецептора VEGF, который регулирует митогенез, ангиогенез и процессы перестройки цитоскелета [18]. Эта усиленная экспрессия рецептора KDR, по всей видимости, и является ключевой причиной для резкого увеличения проницаемости сосудов в условиях СГЯ. Схематично патогенетическая роль эндотелия в условиях СГЯ отображена на рис. 1. Непрерывность архитектоники цитоскелета в эндотелиальных клетках является важным фактором сохранения функций эндотелиального барьера. Проницаемость эндотелия для воды и солей зависит от формы и конфигурации эндотелиоцитов. Эта же группа ученых выявила нарушение регулярности эндотелиального слоя, перестройку активных филаментов и морфологические изменения в эндотелиоцитах под действием ХГЧ. В то же время сам по себе эстрадиол не способен индуцировать экспрессию рецепторов VEGF и не повышает сосудистую проницаемость. Таким образом, блокада VEGF или его рецептора с использованием, например, специфических антител, может быть привлекательной мишенью для разработки новых методов для профилактики и лечения СГЯ.
Рисунок 1.
Роль эндотелиальных клеток в патогенезе СГЯ

VEGF- сосудистый эндотелиальный фактор роста, KDR- рецептор VEGF, ИЛ-6 - интерлейкин-6, ХГЧ - хорионический гонадотропин человека
Таким образом, основную гипотезу развития СГЯ в настоящее время можно представить следующим образом (рис. 2). В условиях СГЯ происходит нарушение регуляции процесса овуляции, что сопровождается гиперпродукцией провоспалительных факторов в яичниках. В результате происходит вторичное увеличение проницаемости капилляров и переход воспалительных медиаторов в другие компартменты. При наиболее тяжелых формах СГЯ этот процесс сопровождается системными проявлениями.
Рисунок 2.
Патофизиология СГЯ

sVCAM-1 - растворимая молекула сосудистой адгезии-1, TNF- фактор некроза опухолей,VEGF- сосудистый эндотелиальный фактор роста,VEGFR-1 - рецептор сосудистого эндотелиального фактора роста, vWF- фактор фон Виллебранда
Классификация СГЯ была предложена RabauE. в 1967 году. Он выделял три клинических категории СГЯ (легкий, средней тяжести, тяжелый) и шесть степеней тяжести, выделенных на основании клинических и лабораторных признаков. В дальнейшем эта классификация была модифицирована MathurR и соавт. (2007) [28]:
Таблица 3.
Классификация СГЯ
| Легкий СГЯ | вздутие живота
слабо выраженная боль в животе увеличение яичников до <8 см |
| СГЯ средней тяжести | умеренно выраженная боль в животе
тошнота +/- рвота увеличение яичников до 8-12 см наличие признаков асцита по данным УЗИ |
| СГЯ тяжелой степени | клинически выраженный асцит (в ряде случаев плевральный выпот)
олигурия гемоконцентрация (гематокрит >45%) гипопротеинемия увеличение яичников >12 см |
| Критический СГЯ | напряженный асцит или массивный плевральный выпот
гемоконцентрация (гематокрит >55%) лейкоцитоз >25000 олигурия/анурия тромбоэмболические осложнения острый респираторный дистресс-синдром |
Критериями тяжести СГЯ является нарушение функции печени, гемоконцентрация, лейкоцитоз, почечная недостаточность, анасарка. Выделяют также жизнеугрожающий или критический СГЯ, который включает в себя увеличение размера яичников, развитие острого респираторного дистресс-синдрома, напряженного асцита, гидроторакса, анасарки, перикардиального выпота, тяжелой почечной недостаточности и тромбоэмболические осложнения. Критерии тяжести СГЯ суммированы в табл. 4.
Таблица 4.
Критерии тяжести СГЯ
| Тяжелый СГЯ | Жизнеугрожающий СГЯ |
| Увеличения размера яичников
Асцит, гидроторакс, анасарка Гематокрит >45% Лейкоцитоз >15 000 Олигурия Креатинин до 1,6 мг/дл Скорость клубочковой фильтрации >50 мл/мин Дисфункция печени |
Увеличения размера яичников
Напряженный асцит, гидроторакс, анасарка Гематокрит >55% Лейкоцитоз >25 000 Креатинин >1,6 мг/мл Скорость клубочковой фильтрации <50 мл/мин Тромбоэмболические осложнения Острый респираторный дистресс-синдром |
СГЯ обычно развивается примерно через 20 дней (в период от 5 до 45 дней) после индукции овуляции [19]. Выделяют раннее начало синдрома - через 3-5 дней назначения овуляторных доз ХГЧ, и позднее начало СГЯ. Последнее бывает обусловлено нарастанием ХГЧ в условиях наступившей беременности и клинически является более тяжелой формой.
Клинические проявления СГЯ
СГЯ является тяжелым осложнением стимуляции овуляции, которое может привести в том числе и к фатальному исходу. С момента внедрения гонадотропинов в клиническую практику для индукции овуляцию был зарегистрирован целый ряд смертельных случаев, косвенно или напрямую связанных с СГЯ. Впервые летальный случай был описан в 1951 году Gotzsche, который сообщил о фатальном артериальном тромбозе - тотальной окклюзии левой внутренней сонной артерии у 37-летней пациентки с бесплодием, получавшей терапию гонадотропином. В последующем были описаны и другие летальные случаи, связанные с СГЯ, когда причиной смерти была массивная тромбоэмболия и ишемический инсульт (Mozws, 1965, Cluroe 1995). Таким образом, тромбозы и эмболии можно рассматривать как наиболее тяжелые осложнения СГЯ, которые могут привести к летальному исходу, инвалидизации вследствие инсульта и ампутации конечностей.
Массивный переход жидкости в интерстициальное пространство характеризуется развитием асцита, гидроторакса, перикардиального выпота, электролитными нарушениями, олигурией, гемоконцентрацией, гиповолемическим шоком. Первым проявлением СГЯ обычно бывают дискомфорт в животе, тошнота, рвота, диарея. Развитие диареи и рвоты, возникновение одышки, одышки, асцита в течение первых 48 часов после назначения ХГЧ свидетельствуют о тяжелом течении заболевания. При физикальном обследовании обнаруживается прибавка массы тела, увеличение объема живота, симптомы гиповолемии. Через брюшную стенку пальпируются увеличенные яичники. Особое внимание следует уделить осмотру конечностей и шеи, чтобы не пропустить тромбоз.
Данные лабораторных исследований свидетельствуют об электролитных нарушениях (гиперкалиемия и гипонатриемия), гемоконцентрации, гипоальбуминемии, повышении уровня креатинина. Примерно у 30% пациенток выявляются нарушения функции печени (умеренная гиперферментемия). При СГЯ вследствие перехода плазмы крови в экстравазальное пространство происходит значительное снижение уровня IgG и IgA в плазме крови, что делает пациентов с СГЯ чувствительными к развитию инфекционных осложнений. При анализе асцитической жидкости выявляется высокая концентрация белка, низкое содержание лейкоцитов и высокий уровень эритроцитов. При ультразвуковом исследовании выявляются множественные фолликулярные кисты и асцит.
Причиной развития дыхательной недостаточности при СГЯ могут служить компрессия легких вследствие асцита, плеврита, перикардиального выпота, развития ОРДС, тромбоэмболии, отека легких, ателектаза, внутриальвеолярных кровоизлияний. В большинстве случаев плевральный выпот развивается с двух сторон и наблюдается одновременно с асцитом. Однако описаны случаи возникновения одностороннего плеврального выпота в качестве единственного симптома СГЯ. Односторонний выпот чаще развивается с правой стороны.
Интересно, что если при спонтанно наступившей беременности тромбозы затрагивают преимущественно (в 70% случаев) глубокие вены нижних конечной (илиофеморальный сегмент), то тромбозы, возникающие вследствие индукции овуляции, локализуются в основном в венах верхней части тела. Хотя увеличение размеров яичников при СГЯ, казалось бы, способствует стазу крови в тазовых венах и венах нижних конечностей. В большинстве случаев (60%) тромбозы, связанные с ЭКО, развиваются в яремной вене, подключичной, подмышечной венах, а также венах головного мозга. Последнее является наиболее тяжелым осложнением. Летальность при тромбозе церебральных вен достигает 5-30%, при этом более опасны тромбозы синусов головного мозга. Интересно, что исход тромбозов церебральных вен у беременных и в послеродовом периоде более благоприятный, чем при церебральных тромбозах, не связанных с беременностью. Полное выздоровление, по данным анализа OuY. и соавт. (2003), наблюдалось у 49% женщин с церебральными тромбозами и у 79% с тромбозами других локализаций [12]. В большинстве случаев развиваются венозные тромбозы, однако у 25% пациентов могут иметь место и артериальные тромбозы (в основном инсульты). В 75% тромбозы развиваются у пациенток с наступившей беременностью, у 66% выявляется СГЯ [12].
По данным KodamaH. и соавт. (1996), маркеры активации коагуляции и фибринолиза (ТАТ, РАР) остаются повышенными после индукции овуляции на протяжении 3-4 недель у женщин с наступившей беременностью [4]. Поэтому развитие тромбоэмболических осложнений возможно и после купирования симптомов СГЯ. В течение первых двух дней после стимуляции овуляции активируется коагуляционный каскад и лишь потом фибринолитическая система. Ранняя активация коагуляции, возможно, является причиной развития субклинических тромбозов. Вероятно, меньший диаметр церебральных сосудов объясняет более раннее развитие клинических проявлений при тромбозах данной локализации (в среднем через 10 дней после стимуляции овуляции). Множественные тромбозы мелких сосудов мозга могут протекать практически бессимптомно или проявляться в виде стертой неврологической симптоматики [29], кроме того, при аутопсии выявляются множественные тромбозы с вовлечением сосудов мозга различного диаметра [30].
Возникновение тромбозов связывают с повышением уровня эстрадиола в крови, гемоконцентрацией и гиповолемией. При повышении уровня эстрогенов возрастает содержание тромбоцитов, фибриногена, vWF и снижается уровень ATIII. Вследствие гемоконцентрации увеличивается вязкость крови и концентрации факторов коагуляции.
Тромбоэмболические осложнения при СГЯ чаще развиваются у пациенток с генетическими формами тромбофилии (дефицит протеинов С, S, ATIII) [12]. Поэтому расширенное исследование системы гемостаза с определением генетических форм тромбофилии и маркеров АФС у пациенток с СГЯ мы считаем обязательным.
Лечение СГЯ
Специфическое лечение СГЯ отсутствует, и терапия сводится в основном к симптоматической. Симптомы СГЯ обычно проходят самостоятельно с уменьшением уровня ХГЧ (в течение 7 дней у небеременных и в течение 10-20 дней у беременных пациенток). Пациенткам требуется полный покой и строгий постельный режим в течение 2-3 недель.
Ежедневно требуется контроль массы тела, диуреза. Рекомендуется выпивать в день более 1 литра жидкости, содержащей электролиты. При среднетяжелом и тяжелом СГЯ следует избегать проведения влагалищного обследования в связи с риском разрыва киста яичника и развития кровотечения. Требуется ежедневный контроль креатинина, электролитов, гематокрита, гемоглобина, клеточного состава крови, печеночных ферментов, коагулограммы, по возможности - бета-ХГЧ [37]. Желательно установить подключичный катетер, что связано с меньшим риском развития тромботических осложнений, чем наличие периферического катетера. При развитии дыхательной недостаточности при отсутствии плеврального выпота или при сомнительных результатах рентгенографии легких требуется исключение ТЭЛА (КТ, вентиляционно-перфузионная сцинтиграфия). Обязательным компонентом лечения является инфузионная терапия. Ее задачами является восстановление ОЦК, ликвидация гемоконцентрации, борьба с почечной недостаточностью. Предпочтительно вводить физиологический раствор и глюкозу. Восстановление электролитного баланса, повышение осмотического давления крови способствует переходу жидкости из внеклеточных пространств обратно в сосудистое русло. При выраженной гиповолемии, гемоконцентрации (гематокрит >45%), гипоальбуминемии (<3 г/дл) рекомендуется применение альбумина и/или свежезамороженной плазмы, которая позволяет также коррегировать показатели системы гемостаза. Важно отметить, что применение диуретиков в условиях гиповолемии и гемоконцентрации, а также их передозировка увеличивают риск развития тромбоэмболических осложнений.
При плевральном выпоте обычно проводится консервативное лечение. Плевральная функция показана при прогрессировании дыхательной недостаточности. Асцит также рекомендуется вести консервативно. Показаниями к парацентезу является напряженный асцит, почечная недостаточность, резистентная к консервативной терапии. Парацентез проводится трансабдоминально или трансвагинально под контролем УЗИ, что позволяет снизить риск повреждения увеличенных яичников. Восстановление функции почек после парацентеза связывают с восстановлением перфузии почек, венозного оттока, нормализацией сердечного выброса. У пациенток с тяжелым СГЯ нередко приходится выполнять парацентез 2-3 раза в неделю. Abuzeid М. и соавт. (2003) предложили применять у таких пациенток постоянный катетер по типу хвоста свиньи [31]. Также при тяжелом СГЯ было предложено наложение перитонеально-венозных шунтов, что позволяет возвращать перитонеальную жидкость в сосудистое русло. При этом удается восполнить потери иммуноглобулинов [12].
В связи с повышенным риском развития инфекционных осложнений у пациенток c СГЯ целесообразным является профилактическое назначение антибиотиков. Риск инфекционных осложнений можно снизить, применяя инвазивные процедуры (лапарацентез, плевральную пункцию) строго по показаниям. Следует отметить, что в 50% случае AbramovY. и соавт. (1998) не выявили возбудителей у пациенток с признаками развития сепсиса [32]. Это может быть связно с тем, что само течение СГЯ является проявлением синдрома системного воспалительного ответа, связанного с массивным выбросом цитокинов и играющего ведущую роль в развитии состояния гиперкоагуляции.
Обязательным является профилактическое назначение антикоагулянтов под контролем маркеров тромбофилии (D-димер) [38]. Препаратом первого выбора для лечения тромботических осложнений СГЯ является НМГ. НМГ должны назначаться всем пациенткам, находящимся на стационарном лечении по поводу СГЯ. При стойкой тяжелой неврологической симптоматике, тромбозе венозных синусов возможно проведение прицельного тромболизиса и тробэктомии. Целесообразно проводить скрининг на наличие генетических форм тромбофилии и АФС, особенно у женщин с тромботическими осложнениями, а также профилактическое применение НМГ у таких пациенток. Важно обеспечить адекватную инфузионную терапию для снижения гемоконцентрации.
По последним данные, учитывая патогенез СГЯ с развитием гиперкоагуляции, воспаления, ДВС-синдрома, возможным эффективным методом терапии может быть применение рекомбинантного активированного протеина С, который уже доказал свою эффективность при тяжелом сепсисе [33]. Однако эта гипотеза требует дальнейших подтверждений.
Сообщается также о новых подходах к лечению СГЯ, которые основаны пока преимущественно на данных экспериментальных исследований на животных. Для терапии СГЯ, в частности, предается применять индометацин, блокирующий синтез простагландинов, которые могут быть одним из патогенетических факторов развития СГЯ. Однако в ретроспективном исследовании BorensteinR. и соавт. (1989) преимуществ использования индометацина показано не было [34]. Более того, в настоящее время применение нестероидных противовоспалительных препаратов при СГЯ не рекомендуется, так как они могут оказывать неблагоприятное влияние на процессы имплантации и усугубить развивающиеся в условиях тяжелого СГЯ нарушения функции почек [35]. Одной из теорий патогенеза СГЯ является выброс гистамина и гистаминоподобных субстанций из яичника. Отчасти эту теорию подтверждает тот факт, что аллергии являются фактором риска развития СГЯ. В исследованиях на животных антигистаминные препараты были эффективными для предотвращения развития СГЯ [36], однако для подтверждения этих предположений требуются проспективные исследования с участием человека.
Резекция яичников при СГЯ категорически противопоказана. Хирургической вмешательство, предпочтительно лапароскопическое, необходимо только при разрыве кисты яичника, перекруте кисты, кровотечении. Перекрут кисты яичника следует заподозрить при появлении болей в нижнем отделе живота и обнаружении уплотненного болезненного образования при пальпации. Снижение гематокрита может быть связано с восстановлением ОЦК, однако прежде всего при этом следует исключать развитие кровотечения.
Редко при неэффективности консервативного лечения при тяжелом течении СГЯ для снижения уровня ХГЧ требуется прерывание беременности.
Профилактика СГЯ включаетвведение ХГЧ только при приемлемом уровне эстрадиола, применение прогестерона, а не ХГЧ в лютеиновую фазу. Кроме того, нами была разработана схема профилактики тромбоэмболических осложнений при подготовки и проведении программ вспомогательных репродуктивных технологий.
Рекомендации по профилактике тромбозов у пациенток, включенных в программы ЭКО
При планировании ЭКО к выбору профилактики венозных тромбоэмболических осложнений следует подходить индивидуально, взвешивая все факторы риска. Особое внимание необходимо уделить оценке состояния системы гемостаза, включая наследственные и приобретенные формы тромбофилии. Согласно международным рекомендациям (табл. 5) введение НМГ следует начинать с утра в день стимуляции овуляции гонадотропинами. Для сведения к минимуму геморрагических осложнений во время забора яйцеклетки в день процедуры НМГ вводить не следует; инъекции НМГ возобновляют на следующий день. В день переноса эмбриона с утра НМГ не вводится. Затем НМГ применяют в профилактических дозах вплоть до подтверждения беременности. В случае наступления беременности профилактическую антикоагулянтную терапию продолжают.
Таблица 5.
Рекомендации по профилактике тромбоэмболических осложнений у женщин, включенных в программы ЭКО
| Клиническая ситуация | Тактика ведения |
| Один эпизод ВТЭ в анамнезе, не связанный с беременностью или приемом оральных контрацептивов), возникший на фоне транзиторных факторов риска и при отсутствии дополнительных факторов риска, например, ожирения | Динамическое наблюдение или профилактические дозы НМГ (эноксапарин 40 мг, фраксипарин 0,3 мл, фрагмин 5000 МЕ один раз в день) +/- компрессионное белье |
| Один идиопатический эпизод ВТЭ в анамнезе или один эпизод ВТЭ в анамнезе при наличии тромбофилии у пациенток, не получающих постоянную антикоагулянтную терапию, или один случай ВТЭ в анамнезе при наличии дополнительных факторов риска (например, ИМТ >35) | Профилактические дозы НМГ (эноксапарин 40 мг, фраксипарин 0,3 мл, далтепарин 5000 МЕ один раз в день) до стимуляции овуляции и в течение всей беременности +/- компрессионное белье. При дефиците антитромбина необходимо назначение более высоких доз НМГ (эноксапарин 0,5 1 мг/кг, далтепарин 50-100 МЕ/кг каждые 12 часов) |
| Более одного эпизода ВТЭ в анамнезе при отсутствии данных о тромбофилии у пациенток, не получающих постоянную антикоагулянтную терапию | Профилактические дозы НМГ до стимуляции овуляции и в течение всей беременности + компрессионное белье |
| Один или более эпизодов ВТЭ в анамнезе у пациенток, получающих постоянную антикоагулянтную терапию (например, при наличии тромбофилии) | Переход с пероральных антикоагулянтов на НМГ (эноксапарин 0,5 1 мг/кг, далтепарин 50-100 МЕ/кг каждые 12 часов) до контролируемой стимуляции овуляции, продолжение применения НМГ в течение всей беременности + компрессионное белье |
| Подтвержденная тромбофилия при отсутствии ВТЭ в анамнезе | Динамическое наблюдение или профилактические дозы НМГ +/- компрессионное белье. Профилактику настоятельно рекомендуется проводить при наличии дефицита антитромбина III, кроме того, лечение в пользу активного ведения следует принять при наличии симптомных ВТЭ в семейном анамнезе и дополнительных факторов риска |
| Наличие факторов риска ВТЭ при отсутствии тромбофилии и ВТЭ в анамнезе | Необходимо проведение индивидуальной оценки риска. При наличии нескольких факторов риска, включая высокий ИМТ, гиподинамию, тяжелые формы гестоза в анамнезе решение следует склонить в пользу активной профилактики: профилактические дозы НМГ +/- компрессионное белье. При высоком ИМТ может потребоваться коррекция дозы НМГ |
| Синдром гиперстимуляции яичников | Профилактические дозы НМГ +/- компрессионное белье. При отсутствии наступления беременности антикоагулянтная терапия может быть закончена после разрешения симптомов. В случае наступления беременности применение НМГ следует продолжить минимум до конца первого триместра. А в дальнейшем в зависимости от показателей системы гемостаза и наличия дополнительных факторов риска ВТЭ |
| Развившаяся ВТЭ | Терапевтические дозы НМГ (например, 1 мг/кг эноксапарина или 90 МЕ/кг далтепарина каждые 12 часов). Антикоагулянтная терапия должна быть продолжена в течение не менее 6 недель после родов |
Нами разработана тактика подготовки к ЭКО и ведения беременности у пациенток с бесплодием и тромбофилией. При подготовке пациенток с бесплодием, с повторными неудачами ЭКО и тромбофилиями к программе ЭКО мы проводим дифференцированную противотромботическая профилактику в зависимости от причины тромбофилии и степени ее выраженности, а также гирудотерапию в течение 1,5 месяца до программы ЭКО. В качестве антитромботической терапии мы используем низкомолекулярный гепарин, начиная с фертильного цикла, а именно в процессе стимуляции овуляции. Терапия отменяется за сутки до планируемой пункции и через 12 ч. после подсадки эмбрионов возобновляется. Также параллельно мы назначаем минидозы аспирина 50-75 мг 1 раз в сутки, начиная с фертильного цикла в зависимости от агрегационной активности тромбоцитов. Всем женщинам назначаются витамины, полиненасыщенную жирную кислоту (омега-3) и антиоксиданты. В случае обнаружения MTHFR C667T обязательно дополнительно назначение фолиевой кислоту (4 мг/сут), а также витамины группы В. Низкомолекулярные гепарина мы применяем на протяжении всей беременности, за сутки до родов (кесарево сечение) препарат отменяется, через 8 ч. терапия возобновляется до 10-го дня послеродового/послеоперационного периода. Контролем эффективности противотромботической терапии служат маркеры тромбинемии и фибринообразования (ТАТ, F1+2, D-димер). Начало программы ЭКО у пациенток с тромбофилией, как наследственной, так и приобретенной, в условиях выраженной активации системы гемостаза и/или повышенных уровней антифосфолипидных антител мы считает противопоказанным до проведения адекватной подготовки к беременности с применением антикоагулянтной терапии и нормализации или улучшения показателей системы гемостаза.
Определение пола ребенка до рождения
В наше время традиционные вопросы при встрече с будущей мамой примерно такие: «Ты ждешь ребенка? А кого, мальчика или девочку?» Вопрос «Кого ждем?» - самый часто задаваемый.. И даже если будущей маме на самом деле все равно, родится у нее мальчик или девочка, к концу девятого месяца ей тоже начнет казаться, что все ее недомогания, капризы, причуды аппетита и внешние метаморфозы зависят не от состояния здоровья или перемены погоды, а исключительно от пола поселившегося внутри нее малыша.
в конце августа как обычно пришли критические дни и по расписанию ушли. через неделю снова пришли и еще на неделю - перепугалась и побежала к геникологу.
там в срочном порядке все рассмотрели в лупу, взяли кучу анализов, отправили на УЗИ - чисто, но странно.
но раз чисто, значит все в порядке.
но раз таки пришла и раз таки все проверили - решила спросить у гениколога о наболевшем. мол пытаемся размножиться, а все никак. как бы это так бы сделать, чтоб все было так, какбы чтобы все получилось - поинтересовалась я.
мне тут же выписали пачку направлений на анализы. гормоны-фирмоны и прочие радости женской жизни.
и само собой эти анализы сдаются в определенный период цикла. вобщем дали пачку, хронометр и отпустили с Богом.
ну так как у меня вот только-только случилось нарушение цикла и фиг знает когда придет следующий я расслабилась и решила съездить с мужем в отпуск.
после отпуска что-то вдруг стало заносить на поворотах и зверски тошнить и по утрам и днем и вечером. но так как у меня с детства такое состояние - практически хроническое, то особо внимания не обратила. сижу с пачкой направлений и жду цикла.
а Германа цикла все нет ... на работе с коллегой болтали на эту тему. у нее тоже задержка, вот она и сказала - видимо вместе в декрет пойдем. поржали и забыли. сижу с пачкой - жду..
устала ждать - пошла купила экспресс-тесты. первый - положительный. ВАУ! не верю глазам своим. а как же пачка? она же ждет!
дабы успокоить совесть и закрепить чувство эйфории второй тест сделала - положительный. Но куда девать здоровый цинизм и правду жизни - покупаю третий тест. Положительный.
и вот я здесь. как бы вроде вот оно - а что дальше делать - не понятно 
в планах сдать анализ крови (хгч) и сходить в ЖК.
далее буду искать с кем бы заключить договор на ведение беременности.
баба Яга в панике и это не может не радовать!
Забеременев, женщина сдает множество анализов, причем некоторые даже по несколько раз. Это может стать причиной для беспокойства: может быть, что-то не так? Одним из таких анализов, которые, возможно, придется сдавать неоднократно, является анализ ХГЧ при беременности.
Что такое ХГЧ
ХГЧ (хорионический гонадотропин человека) – это гормон, выделяемый хорионом после прикрепления оплодотворенной яйцеклетки к стенке матки. Происходит это практически с момента зачатия, поэтому именно ХГЧ является надежным показателем при ранней диагностике беременности, при условии, что результат анализа является достоверным.
Тогда для чего измеряется уровень ХГЧ при беременности не только в 1-м, но и во 2-м, и даже 3-м триместре? Дело в том, что существуют определенные нормы показателей ХГЧ в различные периоды беременности, позволяющие выяснить, нормально ли она протекает и нет ли у плода каких-нибудь патологий.
В состав ХГЧ входят альфа- и бета-частицы. Именно бета-единица имеет уникальную структуру, поэтому имеет значение как раз b-ХГЧ при беременности. Данное лабораторное исследование может проводиться уже на 2-3 день задержки менструации, если зачатие произошло, и с этого момента прошло уже 6-10 дней, уровень ХГЧ обязательно будет повышенным. Если нужна более высокая точность, рекомендуется повторение анализа и ультравагинальное УЗИ.
Кстати, домашние экспресс-тесты на беременность (что бы мы без них делали?) тоже основаны на выявлении ХГЧ при беременности, правда, на гормон, содержащийся не в крови, а в моче, где его концентрация вполовину ниже, поэтому и точность такого метода уступает лабораторному обследованию, но все же является достаточно достоверной.
Уровни ХГЧ при беременности
После оплодотворения яйцеклетки ее внешняя мембрана (хорион) начинает активно выделять гонадотропин, причем очень быстрыми темпами: в 1-м триместре уровень ХГЧ при беременности каждые 2 дня увеличивается вдвое. На 7-10 неделе этот показатель достигает своего пика, а потом постепенно снижается, не изменяясь существенно во 2-й половине беременности. Вот почему по скорости роста ХГЧ при беременности врачи могут судить о ее нормальном развитии или отставании. На 14-18 неделе этот показатель может сигнализировать о развитии патологии. Поэтому назначая этот анализ повторно, ваш врач просто перестраховывается, поэтому не пугайтесь.
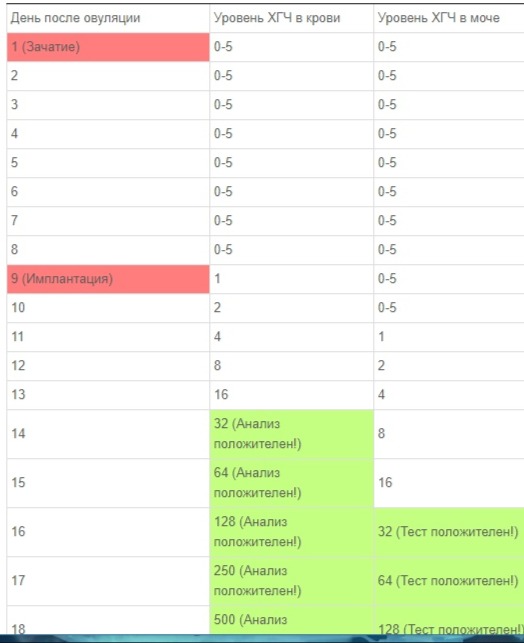
Что же касается норм ХГЧ, то это весьма относительное понятие. Дело в том, что практически в каждой лаборатории установлены свои нормы. Для примера приведем таблицу норм ХГЧ, она поможет вам приблизительно сориентироваться в этом вопросе. Однако помните, что решающие слово о соответствии или отклонениях от нормы ваших анализов, может сказать только квалифицированный специалист.

Нормы уровня ХГЧ по дням после овуляции

Отклонения от нормы ХГЧ при беременности
А что, если анализ ХГЧ при беременности показал некое отклонение от нормы в ту или иную сторону? Конечно, это не слишком хорошо - и повышенный, и пониженный показатель должен насторожить, ведь все это свидетельствует о каких-то проблемах и осложнениях в организме женщины. Главное убедиться, что срок беременности установлен правильно, иначе сравнение с нормой потеряет всякий смысл.
Слишком высокий уровень ХГЧ при беременности – это, в лучшем случае, показатель многоплодной беременности: обычно уровень гормона в крови увеличивается пропорционально количеству эмбрионов.
Кроме того, уровень ХГЧ выше нормы может указывать на следующие патологии:
- ;
- ;
- аномалии развития плода, например, синдром Дауна;
- перенашивание беременности.
Уровень ХГЧ может повыситься, если будущая мать страдает сахарным диабетом и принимает синтетические гестагены.
Ложноположительный результат анализа ХГЧ
Если выясняется, что вы не беременны, а уровень ХГЧ высок (ложноположительный результат анализа), возможно, на него повлиял один из следующих факторов:
- прием некоторых гормональных препаратов, в том числе оральных контрацептивов;
- остаточное явление после предыдущей беременности или аборта;
- хорионкарцинома;
- пузырный занос или его рецидив;
- опухоль яичников, матки, почек, легких.
В любом случае это – повод для обращения к врачу.
Пониженный ХГЧ при беременности может свидетельствовать о внематочной беременности, об угрозе выкидыша, перенашивании. Также это может являться симптомом такого неприятного явления, как хроническая плацентарная недостаточность.
ХГЧ при замершей беременности
Также уровень ХГЧ падает при замершей беременности. Замершая или регрессирующая беременность - это случай, когда плод по тем или иным причинам погиб. Гормон перестает вырабатываться, и анализ показывает падение уровня ХГЧ. Обычно при подозрении на замершую беременность проводится исследования в динамике, то есть анализы сдаются несколько раз, а врач наглядно может определить, как изменяется уровень гормона в крови.
Однако не спешите паниковать – возможно, показатели ХГЧ выходят за пределы нормы для вашего срока беременности лишь потому, что он был установлен неправильно. Такое случается, поэтому для определения регрессирующей беременности назначается УЗИ, только не его основе выносится окончательное заключение. Кроме того, известны случаи, когда при замершей беременности ХГЧ растет, хотя другие признаки уже сошли на нет.
Иногда результаты анализа показывают ХГЧ 0 (отрицательный) при беременности, скорее всего – это тоже ошибка и вам нужно будет сделать анализ повторно.
Как сдавать анализ на ХГЧ
Для того чтобы анализ был максимально точным и достоверным, его нужно правильно сдать. О том, как подготовиться к этому, вам сообщит ваш врач, но знайте, что анализ на содержание в крови b-ХГЧ при беременности сдается натощак. Чаще всего рекомендуют делать это утром, но можно и в другое время суток – при условии, что до этого вы ничего не ели в течение 4-6 часов.
Кровь сдается из вены. За день до этого исключите физические нагрузки – так результат будет более достоверным. Важный момент - если вы принимаете гормональные препараты, они обязательно повлияют на результат анализа, поэтому не забудьте сообщить об этом сотруднику лаборатории, где вы будете сдавать кровь.
В любом случае, даже если результаты анализа на ХГЧ настораживают вас, не спешите паниковать, не делайте далеко идущих выводов – правильно интерпретировать показатели может только врач, который расскажет вам, что делать дальше и, возможно, назначит повторный анализ.
Хорионический гонадотропин человека. Норма ХГЧ при беременности.  Что такое хорионический гонадотропин человека (ХГЧ)?
Что такое хорионический гонадотропин человека (ХГЧ)?
Хорионический гонадотропин человека (ХГЧ) – это особый белок-гормон, который вырабатывается оболочками развивающегося эмбриона в течение всего периода беременности. ХГЧ поддерживает нормальное развитие беременности. Благодаря этому гормону в организме беременной женщины блокируются процессы, которые вызывают месячные и увеличивается выработка гормонов, необходимых для сохранения беременности.
Повышение концентрации ХГЧ в крови и в моче беременной женщины является одним из наиболее ранних признаков беременности.