Гомеопатический подход к бесплодию и его преимущества
Слово «бесплодие» звучит как приговор, однако не стоит опускать руки.
Слово «бесплодие» звучит как приговор, однако не стоит опускать руки.
Метод сравнительной геномной гибридизации на микрочипах (aCGH) позволяет одновременно оценить все 24 хромосомы. Данный метод обладает высокой чувствительностью и точностью и позволяет проводить анализ по единственной клетке. Валидация метода aCGH, по данным литературы, показала его высокую эффективность: только для 2,9% эмбрионов результат анализа не был получен, а уровень ошибки составил 1,9%.
МАТЕРИАЛ И МЕТОДЫ:
Методом аCGH проведена диагностика на 70 бластоцистах у 11 пациенток. Возраст пациенток составил от 25 до 43 лет. Эмбрионы культивировали до 5-го дня, согласно стандартным протоколам лаборатории ЭКО, в индивидуальных каплях на средах фирмы «Origio» в условиях пониженного содержания кислорода (5% О2, 6% СО2). На 4-й день развития всем эмбрионам был выполнен вспомогательный хэтчинг с использованием лазера (Saturn, RI). В случае проведения диагностики на ранее замороженных бластоцистах эмбрионы размораживали накануне, проводили вспомогательный хэтчинг, а биопсию выполняли на следующий день, после чего повторно замораживали. На 5-й день развития на эмбрионах хорошего качества была проведена биопсия клеток трофэктодермы с использованием лазера. Эмбрионы, не достигшие соответствующей стадии развития,
культивировали до 6-го дня для последующей биопсии в случаях, если она становилась возможна. Сразу после проведения биопсии все бластоцисты были заморожены методом витрификации. Дальнейшие преамплификация, амплификация, гибридизация проб и анализ результатов проводились согласно стандартному протоколу (24Sure, BlueGnome).
РЕЗУЛЬТАТЫ:
Результат получен для 64 бластоцист (табл. 2).
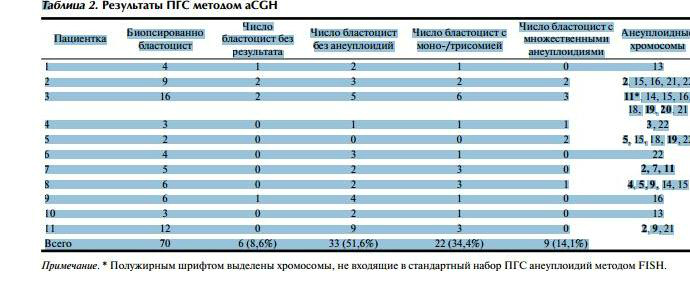
В 6 (8,6%) случаях анализ не проведен вследствие отсутствия амплификации ДНК биопсированного материала. Из 64 проанализированных эмбрионов 33 (51,6%) не имели численных аномалий хромосом, 22 (34,4%) эмбриона имели анеуплоидию по одной из хромосом (моно- или трисомия), у 9 (14,1%) эмбрионов отмечены многочисленные анеуплоидии. Четырем пациенткам выполнен селективный перенос одного размороженного эмбриона после диагностики методом aCGH. В первых двух случаях клиническая беременность подтверждена при ультразвуковом исследовании (УЗИ). Третий перенос - положительный анализ ХГЧ. Результат последнего переноса пока неизвестен. Первый случай беременности - пациентка 40 лет. Клинический диагноз: вторичное бесплодие, эндокринный фактор (гиперпролактинемия, ановуляция), старший репродуктивный возраст. Показанием к проведению предимплантационной диагностики методом CGH явились возраст пациентки и наличие в анамнезе спонтанного выкидыша в сроке беременности 7 нед. Контролируемую овариальную стимуляцию проводили в стандартном длинном протоколе с агонистами ГнРГ (диферелин 0,1 и гонал-Ф). В результате пункции фолликулов получено 15 ооцитов. Диагностика проведена на 9 бластоцистах. Только 3 эмбриона не имели хромосомной патологии. После переноса одного эмбриона наступила прогрессирующая беременность плодом женского пола. В настоящее время проведен УЗИ-скрининг II триместра беременности. Второй случай беременности - пациентка 37 лет. Клинический диагноз: вторичное бесплодие, эндокринный фактор (синдром поликистозных яичников). В анамнезе у пациентки две неразвивающиеся беременности в сроке 5 и 9 нед. Контролируемую овариальную стимуляцию проводили в протоколе с антагонистами ГнРГ (оргалутран, пурегон). В качестве триггера использовали агонист ГнРГ (декапептил). В результате пункции фолликулов получено 43 ооцита. Перенос эмбрионов в лечебном цикле не производили из-за риска развития синдрома гиперстимуляции яичников.У части эмбрионов хорошего качества на 3-й день развития проведена биопсия бластомера с последующей диагностикой методом FISH. По результатам анализа 3 хромосом (X, Y, 21) у 10 (42%) из 24 эмбрионов были выявлены анеуплоидии, 14 (58%) эмбрионов не имели численных отклонений по этим хромосомам и 9 из них достигли стадии бластоцисты и были витрифицированы. Часть эмбрионов, на которых не проводили биопсию бластомера, культивировали до 5-го дня развития. Пять эмбрионов достигли стадии бластоцисты хорошего качества, и на них была проведена биопсия трофэктодермы с последующей aCGH. Первый перенос размороженных эмбрионов проводили с использованием эмбрионов, диагностированных методом FISH. Для переноса были взяты 2 эмбриона хорошего качества, однако беременность не наступила. По результатам aCGH только 2 эмбриона не имели хромосомной патологии. Один из них был перенесен в следующем цикле. На 4-й неделе после переноса биохимическая беременность была подтверждена клинически. При проведении ПГС методом FISH на эмбрионах 3-го дня развития в нашей клинике проводится анализ хромосом 13, 14, 15, 16, 18, 21, 22, X, Y - наиболее часто встречающихся анеуплоидий , при наличии которых возможно рождение ребенка с генетической патологией, а также хромосомной патологии, наиболее часто встречающейся при неразвивающихся беременностях. Однако по результатам метода aCGH, 14 эмбрионов были анеуплоидными по другим хромосомам, и данные эмбрионы не были бы исключены при использовании стандартной методики
FISH и могли быть взяты для переноса, что снизило бы результативность применения программ ВРТ.В дальнейшем планируется накопление и анализ собственных данных.При внедрении методики в хорошо оснащенной
лаборатории, с высокими показателями результативности можно предполагать повышение эффективности программ ВРТ в группах пациенток старшего репродуктивного возраста, пациенток с несколькими предыдущими неудачными попытками ЭКО, а также при носительстве сбалансированных структурных хромосомных аномалий.
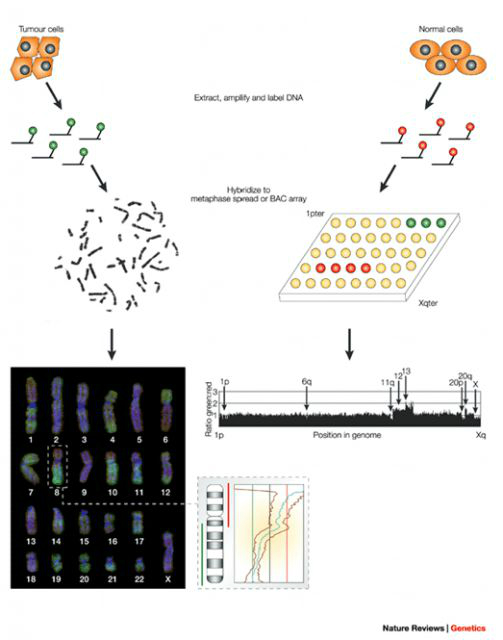
В настоящее время кариотипирование единичных бластомеров или клеток трофэктодермы проводят с помощью сравнительной геномной гибридизации генетического материала, получаемого из этих клеток эмбриона на ранних стадиях его развития, на микрочипе (по-английски Array-based Comparative Genomic Hybridization - aCGH). Микрочип представляет собой миниатюрное стекло (идентичное по размерам обычному предметному стеклу для микроскопа), на которое в строго определенном порядке нанесены фрагменты ДНК различных участков всех хромосом человека. Генетический материал, полученный из исследуемого эмбриона, фрагментируют и метят специальными флуоресцентными красителями, позволяющими впоследствии легко детектировать ДНК. После этого проводят гибридизацию исследуемой ДНК с микрочипом, т. е. с теми фрагментами нормальной ДНК, которые нанесены на него.
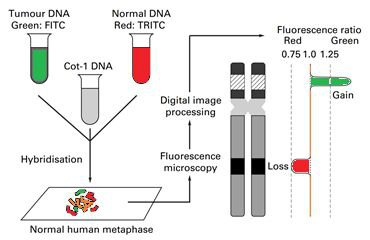
После этого, зная соответствие каждого микрометра поверхности микрочипа определенному фрагменту определенной хромосомы, можно судить о копийности этого локуса в исследуемом образце. Таким образом, проводится анализ потери или наличия лишних хромосом (анэуплоидий), крупных хромосомных перестроек (делеций, дупликаций).
Однако мало кто знает, что столь мощный и высокоразрешающий метод, как aCGH, был разработан и применяется в клинической практике не так давно. Первоначально сравнительная геномная гибридизация заключалась в сравнении паттерна гибридизации меченой ДНК, выделенной из исследуемого биологического образца, с меченной другой краской ДНК, выделенной из нормального контрольного образца, на препарате метафазных хромосом [3]. В норме фрагменты ДНК из исследуемого и контрольного образцов равномерно покрывают окрашенный ими препарат метафазных хромосом, которые в таком случае окрашиваются смешанных цветом. Если в исследуемом образце имеется крупная делеция какого-либо участка (или всей) хромосомы, на метафазных хромосомах в этом месте будет гибридизоваться только контрольная ДНК, что приведет к окраске этого локуса только одной краской, соответствующей нормальной ДНК. Если же какой-то локус (или целая хромосома) окрашен только краской, соответствующей исследуемому образцу, это свидетельствует о том, что данный локус дуплицирован в исследуемом образце или же что имеет место лишняя хромосома.
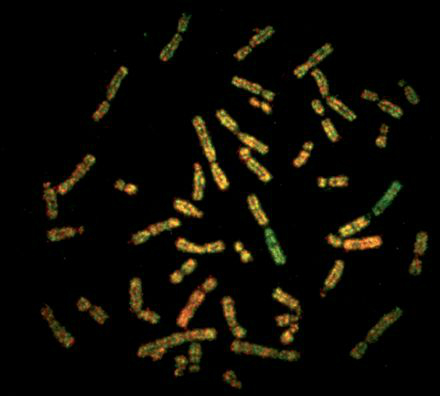
Понятно, что разрешающая способность, т. е. и способность детектировать небольшие перестройки хромосом, метода сравнительной геномной гибридизации на метафазных хромосомах не высока, и с его помощью можно «разглядеть» лишь очень крупные перестройки или диагностировать существенные изменения в кариотипе, как-то: потеря или приобретение целой хромосомы или ее большой части (например, целого плеча).
Разрешающая способность a-CGH (array Comparative Genomic Hybridization), выполняемой на микрочипах, значительно выше. Однако следует различать СГГ, как метод молекуляроного кариотипирования, и как метод детекции анэуплоидий (неправильного числа хромосом). Максимальная чувствительность метода требуется, например, для установления генетической причины заболеваний, сопряженных с делециями, у больных детей. Также сложные случаи пренатальной диагностики, когда нужно установить причину врожденных пороков развития плода, требует СГГ высокого разрешения (молекулярного кариотипирования). С другой стороны, в практике ПГД - преимплантационной генетической диагностики - используется вариант СГГ с меньшим разрешением. Дело в том, что в геноме человека возможно бесконечное количество перестроек, и клиническое значение большинства из них неизвестно. Поэтому такие «случайные находки» происходили бы постоянно, но отбраковывать на основании таких данных эмбрион - неправильно. Основная задача преимпланатационного скрининга - отсеять эмбрионы с заведомо патологическими мутациями, такими, как лишняя или недостающая хромосома, и при этом провести анализ на минимально возможном количестве материала, чтобы не снижать жизнеспособность эмбриона.
Многие современные женщины сталкиваются с проблемами, когда принимают решение завести ребенка. Плохая экология, неправильное питание, малоподвижный образ жизни, постоянные стрессы и недосыпание приводят к тому, что женский организм раньше времени изнашивается, а качество яйцеклеток заметно ухудшается. Поэтому любой представительнице прекрасного пола, которая всерьез настроена стать матерью, необходимо знать о том, какие меры следует предпринять для оздоровления своего организма и для повышения качества яйцеклеток. Ведь только из хорошей яйцеклетки могут развиться здоровые и жизнеспособные эмбрионы, с вынашиванием которых у вас не возникнет ни малейших проблем. Поговорим же об этом более подробно.
Как правило, большинство женщин интересует, как улучшить качество яйцеклеток перед ЭКО. Однако на самом деле озаботиться этим вопросом вы должны независимо от того, планируете ли естественное или искусственное оплодотворение. Так что, начиная планировать наступление беременности, обязательно поговорите со своим лечащим врачом - пусть он сам решит, нужно ли вам сдавать анализ на определение качества яйцеклеток и предпринимать какие-то меры по его улучшению.
Впрочем, существуют некоторые рекомендации, которые помогут любой женщине, даже если она никогда ранее не сталкивалась с проблемами в сфере зачатия. Речь идет об определенных профилактических мероприятиях, к которым относятся:
Ну а если описанных мер будет недостаточно для достижения вашей цели, рекомендуем обратить внимание на специальные медикаментозные препараты и БАДы, которые были разработаны специалистами именно для того, чтобы улучшать качество женских яйцеклеток.
Среди специальных препаратов, предназначенных для повышения качества работы яичников, а также продуцируемых ими яйцеклеток, следует особенно выделить препарат Овариамин. Это вещество, полученное из яичников крупного рогатого скота, которое представляет собой комплекс полезных нуклеопротеидов и белков, способных восстанавливать функцию яичников и нормализовать их работу. Это очень эффективный препарат, который могут принимать женщины всех возрастов. И, если придерживаться инструкции, необходимо принимать ежедневно по 1 - 3 таблетки (или капсулы) препарата за 15 минут до трапезы. Причем ориентировочная продолжительность курса лечения составляет 14 дней, а более точные цифры вам сможет сказать профессиональный гинеколог, к которому вы обратитесь со своей проблемой.
Другие способы улучшения качества яйцеклеток
Способов, которые помогут женщине повысить качество яйцеклеток, существует множество, и выбирать их необходимо в каждом конкретном случае индивидуально, ориентируясь на особенности состояния организма и возраст будущей матери. Ведь иногда женщине, чтобы нормально зачать и выносить ребенка, необходимо принимать такие простые средства, как глицин или фолиевая кислота, а иногда не обойтись и без более серьезных медикаментозных препаратов. Поэтому не стоит работать над улучшением качества яйцеклеток самостоятельно - лучше доверьтесь своему врачу.
Девочки! пусть каждая из нас как можно скорее все это испытает и станет Мамой чудесному сыночку или доченьке!
Весь мир вокруг вдруг изменился
В тот день, когда ты поняла,
Что человечек зародился
Не у кого-то! У тебя!!!
Девочки,взяла с другого сайта)Делюсь с вами!Сама сейчас ориентируюсь по этой табличке...ну оооочень интересно,что происходит с нашими крошками день за днем!
Девочки, а вы знали, что в вк есть такая ? Я посмотрела, у них, оказывается, очень часто проводятся достаточно интересные вебинары:)
а 23го анонсируется вебинар с , тема : "Наиболее эффективные методы лечения бесплодия. " Мне кажется, должно быть очень интересно.
Я же в этот протик больничный не взяла, работаю , а это мне вообще воодушивило
По совету одной знакомой знакомой психологини прочла книгу Риммы Ефимкиной "Как дела? Еще не родила?" о психосоматике бесплодия. Крайне рекомендую.
Она там, правда, крайне радикально прошлась по ЭКО, но, в принципе, если на ситуацию смотреть сверху, а не изнутри (без наших истерик, что не так просто), есть над чем подумать.